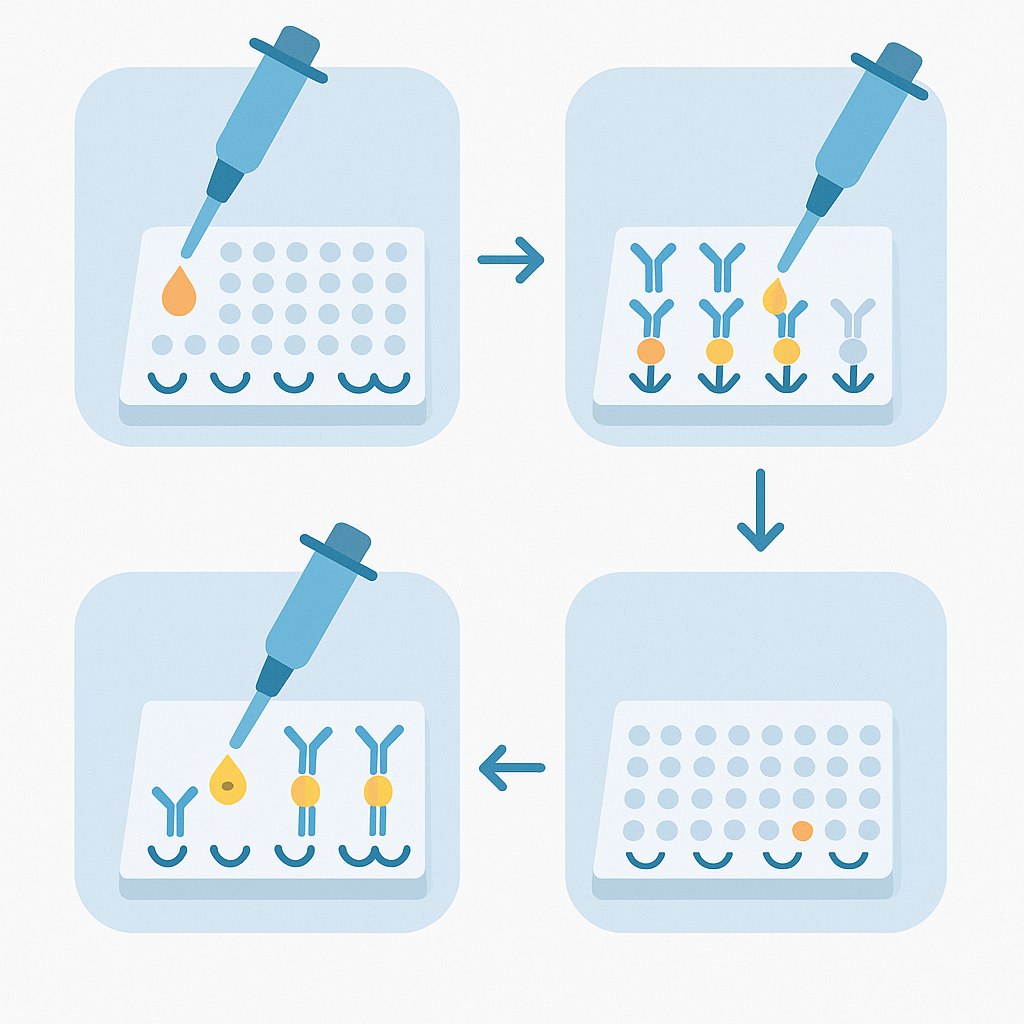
تجزیه و تحلیل کامل مراحل ELISA
مقدمه
آزمون ELISA (Enzyme-Linked Immunosorbent Assay) یکی از روشهای پرکاربرد در علوم زیستی و تشخیص طبی است که بر پایهی واکنش اختصاصی بین آنتیژن یا آنتیبادی انجام میشود.
این روش با بهرهگیری از آنزیمها و سیستمهای رنگزا، امکان شناسایی و اندازهگیری دقیق مولکولهای زیستی را فراهم میکند.
برای درک بهتر عملکرد ELISA، لازم است هر مرحله از این روش بهصورت تحلیلی مورد بررسی قرار گیرد؛ زیرا هر خطا در هر مرحله میتواند بر نتیجه نهایی تأثیر قابل توجهی بگذارد.
آزمون ELISA
پایهی اصلی این روش، اتصال اختصاصی بین آنتیژن (Ag) و آنتیبادی (Ab) است.
یکی از این دو جزء روی سطح جامد (معمولاً پلیت پلیاستایرن) ثابت میشود، و جزء دیگر در محلول قرار دارد. پس از واکنش، یک آنتیبادی کونژوگهشده با آنزیم اضافه میشود که با افزودن سوبسترا، رنگ قابل اندازهگیری تولید میکند.
مراحل اصلی انجام ELISA
روش ELISA معمولاً شامل ۶ مرحله اساسی است. در ادامه هر مرحله را بهصورت تحلیلی بررسی میکنیم:
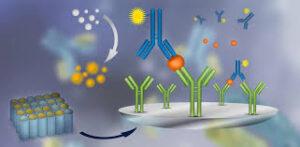 مرحله اول: پوشش آنتیژن یا آنتیبادی روی پلیت (Coating)
مرحله اول: پوشش آنتیژن یا آنتیبادی روی پلیت (Coating)
در این مرحله، آنتیژن یا آنتیبادی اختصاصی روی سطح چاهکهای پلیت ۹۶ خانهای تثبیت میشود.
تحلیل علمی:
-
فرآیند جذب پروتئینها به سطح پلیت به واسطهی برهمکنشهای هیدروفوبیک و الکترواستاتیک انجام میشود.
-
pH و دمای مناسب برای جذب مؤثر پروتئینها بین ۷.۴ تا ۹.۶ است.
-
معمولاً از بافر کربنات–بیکربنات (pH=9.6) استفاده میشود.
خطاهای احتمالی:
-
حجم ناصحیح نمونه → پوشش نامتعادل
-
زمان یا دمای زیاد → دناتوره شدن پروتئینها
پیشنهاد: انکوباسیون در دمای ۴°C طی شب یا ۳۷°C به مدت ۲ ساعت انجام شود.
مرحله دوم: بلوک کردن محلهای آزاد (Blocking)
پس از پوشش، باید سطح پلیت را با مادهای پر کرد تا از اتصال غیر اختصاصی پروتئینها جلوگیری شود.
مواد بلوککننده رایج:
-
BSA (Bovine Serum Albumin)
-
Skim Milk (شیر خشک بدون چربی)
-
Casein یا Gelatin
تحلیل علمی:
این مواد با پوششدادن فضاهای خالی، مانع از اتصال تصادفی آنتیبادیها یا آنزیمها به سطح پلیت میشوند و نویز زمینه (Background Signal) را کاهش میدهند.
نکته مهم:
بلوک کردن مؤثر یکی از کلیدیترین عوامل افزایش اختصاصیت تست است.
مرحله سوم: افزودن نمونه یا آنتیژن هدف (Sample Addition)
در این مرحله، نمونه حاوی آنتیژن یا آنتیبادی مورد نظر به چاهکها اضافه میشود تا با آنتیبادی یا آنتیژن پوشش داده شده واکنش دهد.
تحلیل علمی:
-
زمان و دمای انکوباسیون، بر قدرت اتصال مؤثر است.
-
افزایش دما باعث افزایش سرعت واکنش ولی احتمال کاهش اختصاصیت میشود.
نکات اجرایی:
-
نمونهها باید در بافر رقیقکننده مناسب (PBS یا TBS) آماده شوند.
-
بهتر است نمونهها دو برابر تکرار (Duplicate) آزمایش شوند تا خطاهای احتمالی کاهش یابد.
مرحله چهارم: شستوشو (Washing)
در این مرحله، مواد اضافی و ترکیبات غیر متصلشده با واشر پلیت (Plate Washer) یا شستوشوی دستی حذف میشوند.
تحلیل علمی:
-
هدف از شستوشو، حذف ترکیبات غیراختصاصی است تا سیگنال زمینه کاهش یابد.
-
استفاده از بافر PBS حاوی ۰.۰۵% Tween-20 رایج است.
خطاهای رایج:
-
شستوشوی ناکافی → افزایش نویز
-
شستوشوی بیشازحد → جدا شدن کمپلکسهای ضعیف
پیشنهاد: شستوشو در ۳ تا ۵ چرخه، هر بار با حجم مناسب (۳۰۰ µL در هر چاهک).
مرحله پنجم: افزودن آنتیبادی کونژوگه با آنزیم (Conjugate Addition)
در این مرحله، آنتیبادی ثانویه متصل به آنزیم به چاهک اضافه میشود.
آنزیم متداول معمولاً HRP (Horseradish Peroxidase) یا ALP (Alkaline Phosphatase) است.
تحلیل علمی:
-
این مرحله تعیینکنندهی حساسیت آزمایش است، زیرا هر آنزیم باعث تولید چندین مولکول محصول رنگی میشود (Amplification Effect).
-
زمان واکنش معمولاً بین ۳۰ تا ۶۰ دقیقه در ۳۷°C است.
نکات اجرایی:
-
محلول کونژوگه باید تازه و بهدرستی رقیق شده باشد.
-
تماس مستقیم با نور شدید باعث تخریب HRP میشود.
مرحله ششم: افزودن سوبسترا و قرائت رنگ (Substrate & Reading)
در این مرحله، سوبسترا (مثل TMB یا OPD) به چاهکها اضافه میشود و واکنش آنزیمی باعث تولید رنگ میگردد.
تحلیل علمی:
-
رنگ تولیدی متناسب با مقدار آنتیژن یا آنتیبادی هدف است.
-
واکنش معمولاً در تاریکی و دمای اتاق انجام میشود.
-
سپس با افزودن محلول توقف (Stop Solution) مثل H₂SO₄، واکنش متوقف میگردد.
اندازهگیری:
-
جذب نوری (Optical Density) در طول موج ۴۵۰ nm خوانده میشود.
-
نتایج با منحنی استاندارد مقایسه و غلظت نهایی تعیین میشود.
تجزیه و تحلیل دادهها (Data Analysis)
پس از خواندن جذب نوری توسط دستگاه ELISA Reader، باید دادهها تحلیل شوند:
مراحل تحلیل:
-
رسم منحنی استاندارد (Standard Curve) با استفاده از نمونههای غلظت معلوم.
-
استفاده از رگرسیون خطی یا لجستیک چهار پارامتری (4PL) برای محاسبه غلظتها.
-
حذف دادههای خارج از محدوده (Outliers).
-
محاسبه میانگین نمونههای تکراری.
-
تعیین حساسیت (LOD) و محدوده دینامیکی.
نکته تحلیلی:
اگر اختلاف جذب بین کنترل مثبت و منفی کم باشد، احتمال خطای شستوشو یا تخریب آنزیم وجود دارد.
تجزیه و تحلیل کامل مراحل ELISA
| مرحله | نوع خطا | علت احتمالی | راهحل |
|---|---|---|---|
| پوشش پلیت | جذب ناکامل | غلظت کم پروتئین یا pH نامناسب | افزایش غلظت یا تغییر بافر |
| بلوک کردن | سیگنال بالا | بلوک ناکافی | استفاده از BSA یا شیر خشک تازه |
| شستوشو | نویز زیاد | شستوشوی ناکافی | افزایش دفعات شستوشو |
| افزودن کونژوگه | سیگنال ضعیف | تخریب آنزیم | نگهداری در دمای مناسب و تاریکی |
| خواندن رنگ | جذب غیرخطی | تاخیر در قرائت | خوانش سریع پس از توقف واکنش |
نکات کلیدی برای بهینهسازی ELISA
-
دمای واکنشها را بین ۲۰–۳۷°C کنترل کنید.
-
از نمونههای کنترل مثبت و منفی در هر تست استفاده کنید.
-
از نوک پیپت استریل و یکبارمصرف برای جلوگیری از آلودگی استفاده شود.
-
پلیتها را پس از هر مرحله کاملاً خشک کنید.
-
دستگاه ریدر را هر ۶ ماه یک بار کالیبره نمایید.
نتیجهگیری
آزمون ELISA بهدلیل حساسیت، اختصاصیت و سادگی اجرا، یکی از روشهای طلایی در تشخیص آزمایشگاهی است.
تجزیه و تحلیل دقیق مراحل آن نشان میدهد که کوچکترین خطا در هر مرحله (از پوشش پلیت تا قرائت نهایی) میتواند نتیجه را تغییر دهد.
بنابراین رعایت اصول استاندارد، کنترل کیفی مواد و دقت در تنظیم دستگاهها برای دستیابی به نتایج قابل اعتماد ضروری است.